Atomas yra viskame, ką stebime aplinkui. Kiekvienas gyvas padaras ir negyvi daiktai susideda iš atomų, kuriuose negyvi daiktai susideda iš materijos. Tačiau atomas yra pagrindinis materijos elementas. Taigi, viskas susideda iš atomų. Terminas „Atom“ yra graikų kalbos žodis, kurio reikšmė yra nedaloma. Graikai tikėjo, kad materija gali susitrenkti į labai mažas nematytas daleles, kurios vadinamos atomais. Atomo sąvoką apibūdina graikų filosofai, būtent Democritas ir Johnas Daltonas. Toks filosofas kaip Demokritas paaiškino materijos sampratą ir taip pat numatė, kad visa medžiaga susideda iš materijos. Jis patvirtino, kad atomai nuolat juda, nematomos, mažytės dalelės, kurios nepanašios pagal kontūrą, matmenį ir temperatūra & negalima sutriuškinti. Šiame straipsnyje aptariama atomo struktūros apžvalga.
Kas yra „Atom“?
Apibrėžimas: Pagrindiniai esmės vienetai, taip pat svarbi medžiagos struktūra elementai , vadinami atomais. Kadangi pavadinimas yra paimtas iš graikų kalbos žodžio, reiškiančio neištirpstantį, kadangi atomai yra mažiausi daiktai, kuriuos galima rasti erdvėje, ir jų negalima atskirti. Jie yra išrasti su trimis dalelėmis, tokiomis kaip elektronai, protonai ir neutronai, kurie yra sukurti net su nedidelėmis dalelėmis, būtent su kvarkais. Svarbūs elementai yra vandenilis, helis, azotas, geležis, anglis, chloras, aliuminis ir auksas.

Atomas
Atomo struktūra
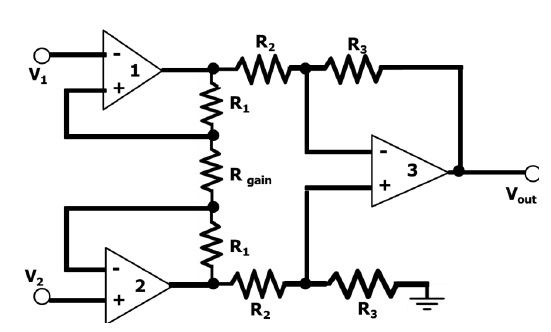
Atomo struktūra daugiausia apima du regionus, būtent centrinį ir išorinį regionus. Centrinis atomo regionas (branduolys) apima protonus ir neutronus, o išorinis elektronai orbitoje branduolio srityje. Protonų ir neutronų masė branduolyje turi maždaug 1,67 × 10–24 gramus. Kiekvienas išorinio regiono elektronas turi -ve krūvį (-1), kuris yra lygus protono + ve krūviui (+1).

Atomo struktūra
Tokie elementai, kaip „Neutronai“, yra nepakrauti, randami branduolyje. Atomai yra mažiausi vienetai, turintys skirtingas chemines elemento savybes. Atomai susijungia ir susidaro molekulės, kurios sąveikauja su kietosiomis medžiagomis, skysčiais ar dujomis. Pavyzdžiui, vanduo gali būti sudarytas iš deguonies ir vandenilio atomų, o abu atomai sujungs vandens molekules.
Elektronų masė yra daug mažesnė, palyginti su protonais, tokiais kaip 9,11 × 10–28 gramai. Tyrėjai nustato tokį masės kiekį kaip 1 AMU (atominės masės vienetas), kitaip - 1 Daltonas. Taigi jie neatiduoda daug bendros elemento atominės masės. Atominėje masėje yra normalu neatsižvelgti į atomų elektronų masę ir masę galima apskaičiuoti remiantis Nr. protonų ir neutronų.
Elektronai labai aukoja atomo krūviui, nes kiekvienas elektronas turi neigiamą krūvį -1), kuris yra lygus teigiamam protono krūviui (+1). Neutronų atome aplink branduolį skriejantys elektronai yra lygiaverčiai Nr. protonų branduolyje.
- Į daleles panašus protonų krūvis yra +1, masė yra 1amu ir yra branduolyje.
- Į daleles panašus neutronų krūvis yra 0, masė yra 1amu ir yra branduolyje.
- Į daleles panašus elektronų krūvis yra -1, masė yra 0 ir yra orbitalėse.
Atominė energija
1930–1940 m. Mokslininkai nustatė, kad jei bomba uranas, įskaitant neutroną, tada branduolys bus padalytas į du tipus. Kai tai įvyksta, energija gali būti išlaisvinta, vadinama branduolio dalijimusi.
Pirmasis branduolio dalijimasis buvo panaudotas atominėse bombose. Antrojo pasaulinio karo metu amerikiečiai numetė šias bombas virš Japonijos šalies. Atominės bombos pagamino tiek energijos, kad nužudytų tūkstančius žmonių. Vėliau mokslininkai ištyrė, kaip šią energiją būtų galima panaudoti nesmurtiniu būdu. 1950 metais buvo suprojektuotas pirmasis atominis reaktorius ir jie generuoja energiją dalijant atomus.
Atomo savybės
Atomo savybės apima atominį skaičių, elektros krūvį, dydį, radioaktyvumą, atomo masę, subatominius elementus, jėgas atome, atomo stabilumą, branduolinę jėgą, atomus, molekules ir medžiagas.
Atominis skaičius
Atomo skaičius yra ne kas kitas, o protono skaičius atome. Pavyzdžiui, vandenilio atominis skaičius yra 1, taigi jis apima vieną protoną. Gamtoje taip pat galima rasti elementų su 92 automatiniais numeriais, nes juos laboratorijoje sudaro mokslininkai.
Atominės Mišios
Ne. protonų ir neutronų, esančių atome, vadinama atomine mase. Atomų su panašiu elementu panašus Nr. protonų. Kartais jie turi daugiau neutronų, todėl tokie atomai vadinami izotopais.
Pavyzdžiui, toks elementas kaip vandenilis apima 3 izotopus. Paprastai tai apima 1 protoną ir 1 neutroną. Kai kuriais atvejais galime rasti vandenilio izotopų, kuriuose yra 2 arba 3 neutronai, tačiau ir jie turi tik vieną protoną.
Lengvesniuose elementuose kiekvieno atomo branduolys apima tą patį Nr. neutronų ir protonų, tuo tarpu sunkesniuose elementuose jie turi mažiau protonų nei neutronai. Pavyzdžiui, urane yra 92 protonai ir 146 neutronai, o urano atominė masė yra 238.
Elektrinis įkrovimas
Paprastai atomas elektriniu požiūriu gali būti neutralus. Tačiau susidūręs su naujais atomais, jis gali prarasti ar įgyti elektronų. Kai šis pelnas ar praranda elektroną, yra žinomas kaip jonas kuris apima elektros krūvį. Kai atomas praranda elektronus, jis taps teigiamais jonais, o atomas - elektronus, tada neigiamu jonu.
Radioaktyvumas
Kai kurių atomų branduolys natūraliai pasikeis, jis vadinamas radioaktyviuoju. Kai branduolys pasikeis, jis gamins spindulius. Gamtoje esantys radioaktyvieji elementai yra radis arba uranas.
DUK
1). Kas yra atomas?
Atomas yra pagrindinė materijos dalis ir susideda iš trijų mažų dalelių rūšių, tokių kaip protonai, elektronai ir neutronai.
2). Kokie yra skirtingi atomų tipai?
Jie yra stabilūs, izotopai, radioaktyvūs, jonai ir antimaterija.
3). Ar galime pamatyti atomus?
Ne, jie nematomi
4). Koks yra atomo centras?
Atomo centras vadinamas branduoliu, į kurį įeina protonai ir neutronai.
5). Koks yra atomo dydis?
Atomo dydis yra 100 pikometrų
Taigi, viskas apie tai atomo struktūros apžvalga . Tai yra pats svarbiausias kasdienio gyvenimo elementas. Visi elementai yra išrasti naudojant atominę fiziką, kuriai priklauso elektronai, protonai ir neutronai. Pasaulis susideda iš materijos, o materija - iš atomų. Taigi visa visata susideda iš atomų. Šiuo metu atomo fizika yra viena reikšmingiausių temų, nes ji turi autoritetą valdyti visuomenę dabartyje ar ateityje. Čia yra klausimas jums, kas išrado atomą?